
Ponencias
21
reclutamiento de CMLVs a través de su receptor CCR2 y facilita
la estabilización de nuevos capilares, formando una red estable y
madura de neovasos
15
(Figura 3)
.
Los procesos angiogénicos están regulados mediante una com-
pleja red de factores de transcripción. ETS1 media la activación de
la transcripción de algunos de los genes reguladores del balance
angiogénico. Este fenómeno suele implicar sinergismos con otros
factores de transcripción. Se han descrito interacciones entre ETS1
y factores de transcripción como AP-1, la proteína de leucemia
mieloide aguda-1 (AML-1), el factor de transcripción E3 (TFE3)
y la proteína de especificidad 1 (SP1). Las proteínas SMAD son
factores de transcripción que a menudo presentan un sinergismo
con otras moléculas reguladoras de procesos celulares. En este sen-
tido, se ha descrito que SMAD3 coopera con ETS1 para regular la
expresión proteica de la hormona paratiroidea en células de cáncer
de mama. La proteína SMAD3 también se ve alterada por la señali-
zación de FT
12
y comparte con ETS1 la capacidad de cooperar con
los factores de transcripción AP-1, AML-1, TFE3 y SP1. A través
de la inhibición y la sobreexpresión de ETS1 y SMAD3, y de ensa-
yos de actividad luciferasa del promotor CCL2, hemos identificado
la cooperación de los factores de transcripción ETS1 y SMAD3 en
la regulación de la expresión génica de CCL2 y en la angiogénesis
mediada por FT
12
. Viendo que, mientras la vía FT/AKT/ETS1 es
independiente de PAR2, la activación de SMAD3 se desencadena
a partir de la interacción de FT y PAR2, de forma independiente
de Akt1. Esta conclusión está muy relacionada con otros estudios
recientes que apuntan que PAR2 activa la vía de SMAD2 por una
transactivación de un receptor de TGF
β
. Las proteínas SMAD
son proteínas intracelulares que transducen señales desde ligan-
dos TGF
β
al núcleo, donde activan una cascada de transcripción
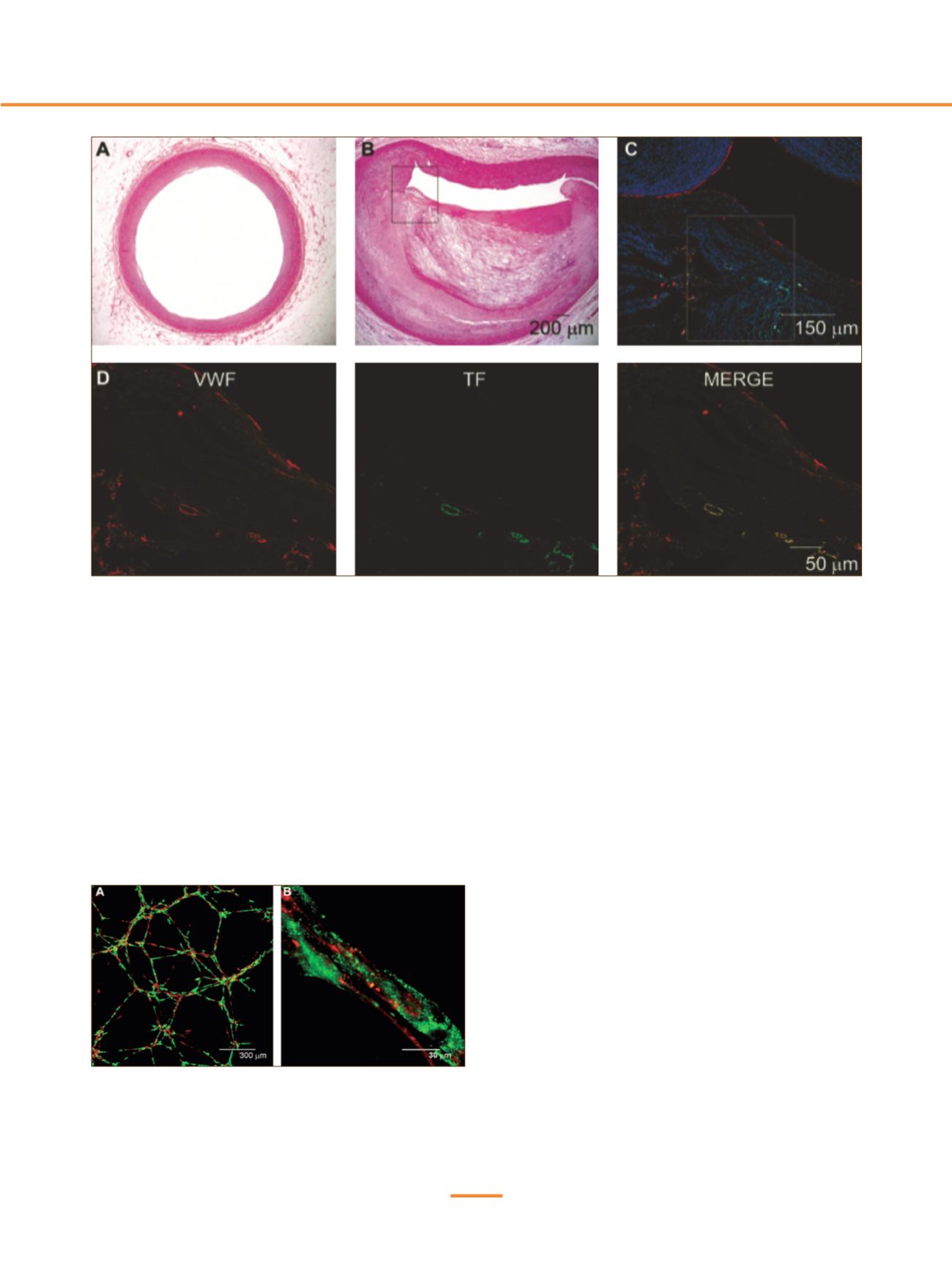
Figura 2.
Estudio de inmunolocalización de angiogénesis y de FT en la placa aterosclerótica.
Las placas ateroscleróticas avanzadas en arterias coronarias humanas muestran una extensa red de microvasos. A) Arteria coronaria humana normal.
Presenta un grosor de la íntima sin alteraciones y no se observan indicios de neovascularización. B) Placa aterosclerótica avanzada en una arteria
coronaria humana. C) Magnificación de B. Los microvasos pueden observarse mediante la tinción inmunofluorescente de vWF, que marca las CEs (rojo)
y Hoescht 33342, que marca los núcleos de las células (azul). D) Doble inmunolocalización de FT (verde), expresado en los microvasos de las lesiones
ateroscleróticas, colocalizando con las CEs (rojo). Adaptado de Arderiu, G. et al., 2011
15
.
Figura 3.
CVML confieren estabilidad a las CE y se situan a su alrededor.
Co cultivo de CEs (rojo) com CVMLs (verde) en un sistema tridimensional
durante 18 horas.



















