
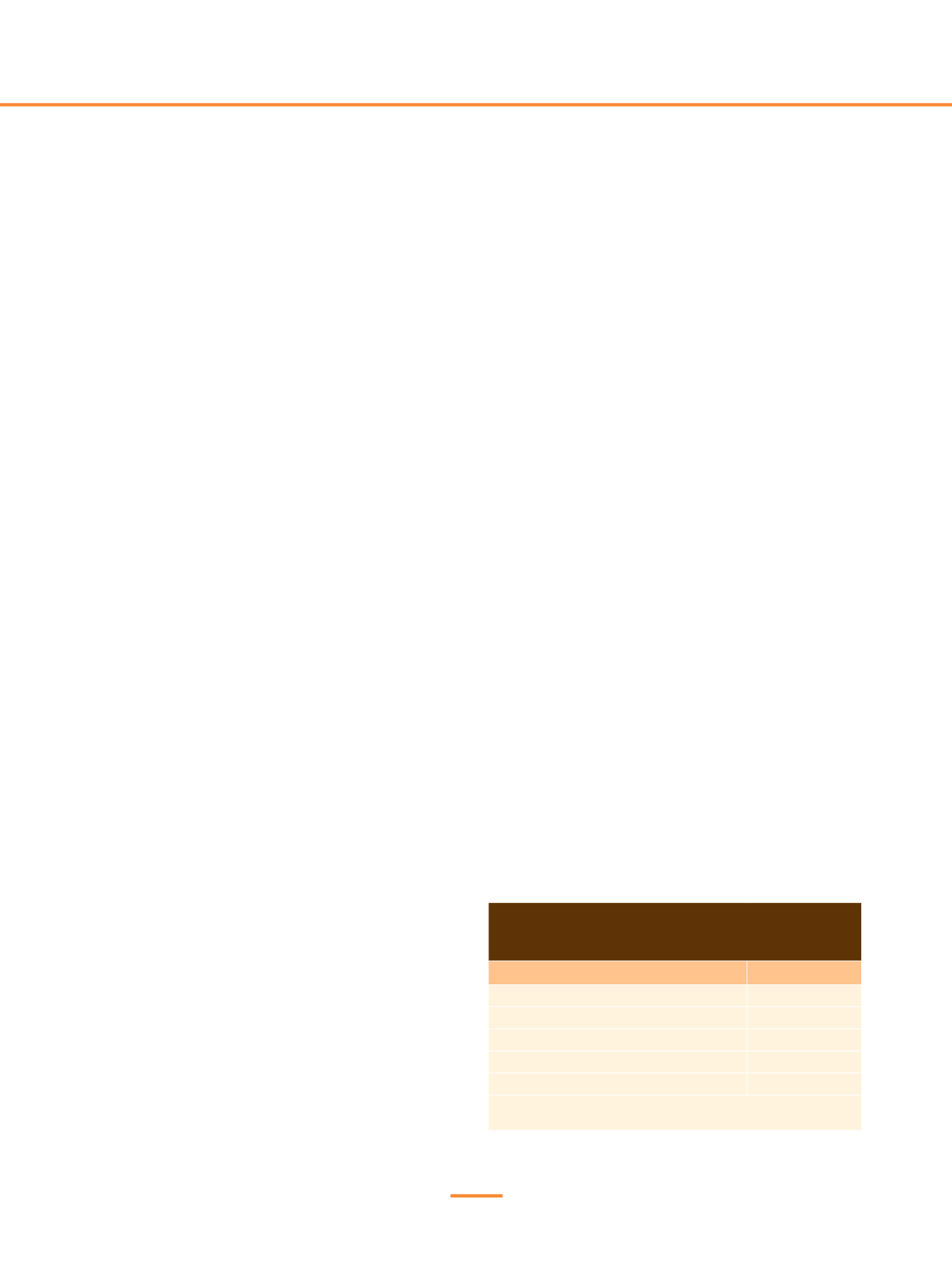
XXXII Congreso Nacional de la Sociedad Española de Trombosis y Hemostasia
52
Globalmente, se puede afirmar que el papel de la trombofilia
hereditaria (excluyendo los raros casos de defectos combinados)
en el riesgo de recurrencia es modesto. De hecho, la trombofilia
no se tiene en cuenta a la hora de las recomendaciones sobre la
duración del tratamiento anticoagulante en las últimas ediciones
de la guía de tratamiento antitrombótico del ACCP
3
. En este sen-
tido, sorprende más que ni siquiera se tenga en cuenta el síndrome
antifosfolípido. Aunque la evidencia disponible al respecto no es
abundante, en la práctica habitual es frecuente anticoagular de
forma prolongada a pacientes con ETEV y anticuerpos antifos-
folípido confirmados
9
, particularmente en el caso de aquellos que
resulten triple positivos o presenten títulos altos. Una aproxima-
ción novedosa ha sido la evaluación de posibles diferencias en
la expresión génica (transciptoma) de pacientes con recurrencia
trombótica y sin ella tras un primer episodio de ETEV no provo-
cada. El estudio RETRO mostró la existencia una expresión dife-
rencial entre ambos grupos de pacientes
10
. El estudio de validación
en una segunda población independiente confirmó una asociación
de la expresión del gen
ACSF2,
implicado en el metabolismo de
los ácidos grasos, con el riesgo de recurrencia. Se desconocen los
posibles mecanismos implicados y sería deseable una confirma-
ción de resultados en estudios con mayor número de pacientes.
Los niveles elevados de dímero-D (DD) al finalizar el tratamien-
to anticoagulante y en los meses posteriores se asocian con un mayor
riesgo de recurrencia. Sin embargo, su valor predictivo positivo es
reducido. La determinación seriada de DD tiene una utilidad relativa
para identificar individuos con ETEV no provocada o asociada a
factores de riesgo débiles con bajo riesgo de recurrencia
11,12
. Dos
problemas en relación con la utilización del DD para este fin son la
insuficiente estandarización y la validación de los puntos de corte
para cada reactivo. Esto último además puede complicarse sobre-
manera si, tratando de buscar una mayor rentabilidad de la técnica,
se buscan puntos de corte ajustados para diferentes tramos de edad.
De forma similar, en la población del estudio
MEGA follow-up
,
los niveles plasmáticos elevados de FVIII tras la finalización de la
anticoagulación también se han asociado con un mayor riesgo de
recurrencia, con HR de 3,4 (IC95% 2,2-5,3) para niveles > 200 UI/dl
frente a < 100 UI/dl
13
. En la práctica clínica habitual resulta compli-
cado que un paciente reinicie la anticoagulación después de haberla
suspendido, lo que lastra la utilidad del DD o del FVIII. Por otra
parte, algunos estudios han descrito una asociación de parámetros
relacionados con la generación de trombina con el riesgo de recu-
rrencia
14
. Sin embargo, la naturaleza técnica de la prueba dificulta
su implementación en laboratorios clínicos de rutina.
La importancia de la persistencia de trombosis residual tam-
bién ha sido motivo de controversia. Al igual que sucedía con
la trombofilia, el papel parce ser modesto (HR de 1,32, IC 95%
1,06-1,65) en un reciente metanálisis
15
, insuficiente para basar las
decisiones únicamente en esta variable. Además, no hay que olvi-
dar la dificultad para evaluar la persistencia de obstrucción venosa
residual en algunos casos y que los criterios diagnósticos no están
claramente definidos.
Por supuesto, la presencia de un cáncer activo es un recono-
cido factor de riesgo de recurrencia en pacientes con ETEV. En la
ETEV asociada a cáncer las principales guías de práctica clínica
recomiendan un mínimo de 3 meses de anticoagulación y prolongar
el tratamiento anticoagulante mientras persista enfermedad activa.
Un reciente estudio ha demostrado la baja tasa de recurrencia en
pacientes curados de la enfermedad neoplásica, y cómo una reci-
diva tumoral constituye un importante factor de riesgo de ETEV
recurrente
16
. Sin embargo, el paciente con trombosis asociada a
cáncer también presenta un riesgo relevante de recurrencia durante
el tratamiento anticoagulante. De hecho, en caso de pacientes con
ETEV no provocada que recurren durante la anticoagulación se debe
descartar la presencia de una neoplasia oculta. Existe una escala
validada (escala de Ottawa,
Tabla 2
) útil para estratificar el riesgo de
recurrencia durante el tratamiento anticoagulante en pacientes con
cáncer
17
, si bien por ahora no se ha demostrado una utilidad para
plantear diferentes esquemas de tratamiento.
Otras situaciones clínicas que se han asociado con un aumento
del riesgo de recurrencia de la ETEV son la obesidad, la enfer-
medad inflamatoria intestinal, el embarazo y el tratamiento estro-
génico (en caso de nueva exposición a dicho factor de riesgo), o
incluso la presencia de sintomatología depresiva
8,18
.
Por último, determinados tratamientos concomitantes, además
de la calidad del propio tratamiento anticoagulante inicial, influyen
en el riesgo de recurrencia. La utilización de filtros en vena cava
inferior aumenta el riesgo de TVP recurrente, tanto si se administra
o no anticoagulación concomitante
19,20
. Por el contrario, el uso
de estatinas disminuye en torno al 40% el riesgo de recurrencia
tromboembólica venosa, si bien se precisa confirmación mediante
ensayos clínicos aleatorizados
21,22
.
Modelos predictivos de ETEV recurrente
A partir de series prospectivas de pacientes con ETEV no
provocada se han desarrollado varios modelos de evaluación del
riesgo de recurrencia que incluyen combinaciones de variables
con distintos pesos relativos. Destacan la escala de Rodger
(Men
continue and HERDOO2
), el modelo predictivo de Viena, la escala
DASH y la reciente escala DAMOVES
23-26
(Tabla 3)
. Ninguna de
ellas ha sido suficientemente validada en diferentes poblaciones de
pacientes y, sobre todo, no existen estudios prospectivos en los que
el manejo clínico de los pacientes se haya basado en su aplicación.
Una posible aproximación práctica
Centrándonos en la ETEV no provocada (no consideramos por
tanto los episodios asociados a tratamiento hormonal o a cáncer),
Tabla 2.
Escala predictiva de recurrencia tromboembólica
durante el tratamiento anticoagulante en pacientes con
trombosis asociada a cáncer (escala de Ottawa)
Factor de riesgo
Puntuación
Sexo femenino
+1
Cáncer de pulmón
+1
Historia previa de ETEV
+1
Cáncer de mama
-1
Estadio inicial (TNM I)
-2
Riesgo bajo = ≤ 0 puntos: recurrencia 4,5% a los 6 meses.
Riesgo alto = ≥ 1 punto: recurrencia 19,1%.



















