
XXXII Congreso Nacional de la Sociedad Española de Trombosis y Hemostasia
90
incluir este desorden en las pruebas de trombofilia para definir el
riesgo trombótico de cada individuo.
Financiación: CB15/00055 (del ISCIII & FEDER); 19873/
GERM/15 Fundación Séneca.
Gammapatías monoclonales
SP-006
Desarrollo de un modelo predictivo de
riesgo de infecciones graves en pacientes
con mieloma múltiple no candidatos a
trasplante autólogo: datos del estudio FIRST
Lahuerta J. J. (1), Dumontet Ch. (2), Hulin C. (3), Dimopoulos M. A.
(4), Belch A. (5), Dispenzieri A. (6), Ludwig H. (7), Rodon P. (8), Van
Doogenbroeck J. (9), Qiu L. (10), Cavo M. (11), Van de Velde A. (12),
Allangba O. (13), Hoon Lee J. (14), Boyle E. (15), Civet A. (16), Costa
B. (17), Tinel A. (17), Gaston-Mathé Y. (16), Facon T. (15)
(1) Hospital Universitario 12 de Octubre. Madrid, Spain. (2) Hospices Civils
de Lyon. Lyon, France. (3) CHU Bordeaux. Bordeaux, France. (4) National and
Kapodistrian. University of Athens. Athens, Greece. (5) Cross Cancer Institute.
Edmonton, AB, Canada. (6) Mayo Clinic Cancer Center. Rochester, MN, USA.
(7) Wilhelminen Hospital. Wilhelminen Cancer Research Institute. Vienna,
Austria. (8) Centre Hospitalier. Périgueux, France. (9) AZ Sint-Jan AV Brugge.
Brugge, Belgium. (10) Blood Disease Hospital. Chinese Academy of Medical
Science and Peking Union Medical College. Tianjin, China. (11) Seràgnoli
Institute of Hematology. Bologna University School of Medicine. Bologna,
Italy. (12) Universitair Ziekenhuis Antwerpen. Edegem, Belgium. (13) Centre
Hospitalier Yves Le Foll. France. (14) Gachon University Gil Hospital. Incheon,
Korea. (15) CHRU Lille. Lille, France. (16) YGM Consult. Quinten. Paris, France.
(17) Celgene International Sàrl. Boudry, Switzerland
Antecedentes:
Los pacientes (pts) con mieloma múltiple
(MM) tienen un mayor riesgo de infecciones debido a la toxici-
dad de los tratamientos, inmunosupresión, comorbilidades, y edad
avanzada. Además, presentan una baja respuesta inmune a la va-
cunación tanto para profilaxis víricas como bacterianas, por lo que
existe una necesidad de medidas preventivas tempranas. El estudio
pivotal FIRST comparó la eficacia de lenalidomida más dosis bajas
de dexametasona (Rd) con la combinación de melfalán, prednisona
y talidomida (MPT) en pts con MM no candidatos a trasplante.
Objetivos:
Identificar los factores predictivos de infecciones
en los primeros 4 meses del estudio FIRST y desarrollar un mo-
delo predictivo de riesgo de infección.
Métodos:
En el estudio FIRST, tras firmar el consentimiento,
los pts fueron aleatorizados a recibir Rd continuo hasta la progre-
sión, Rd x 18 ciclos (Rd18), o MPT. Para el presente análisis, se
combinaron los datos de Rd continuo y Rd18. Se analizaron datos
demográficos, antecedentes y características clínicas basales (in-
cluyendo medicación concomitante) para identificar factores de
riesgo para el tratamiento emergente (TE) grado = 3 de infeccio-
nes durante los primeros 4 meses. Los pts con una supervivencia
libre de progresión (SLP) = 4 meses y sin infecciones TE = 3 du-
rante los primeros 4 meses fueron excluidos. Se utilizó un algorit-
mo de descubrimiento de subgrupos para identificar los factores
asociados con un alto o bajo riesgo de infección. Las variables
clínicas y biológicas más relevantes se utilizaron en un modelo
multivariante de regresión logística con un proceso iterativo de
selección de variables. Los pts con ausencia de datos en al menos
1 variable fueron excluidos (n = 9). A partir del modelo predicti-
vo resultante, se desarrolló un sistema de puntuación mediante la
asignación de -2 a 2 puntos a los factores de bajo o alto riesgo en
función de su influencia en el modelo. La puntuación acumulada
clasificó a los pts en dos grupos: alto riesgo (2 a 5 puntos) o bajo
riesgo (-3 a 1 puntos) de infección.
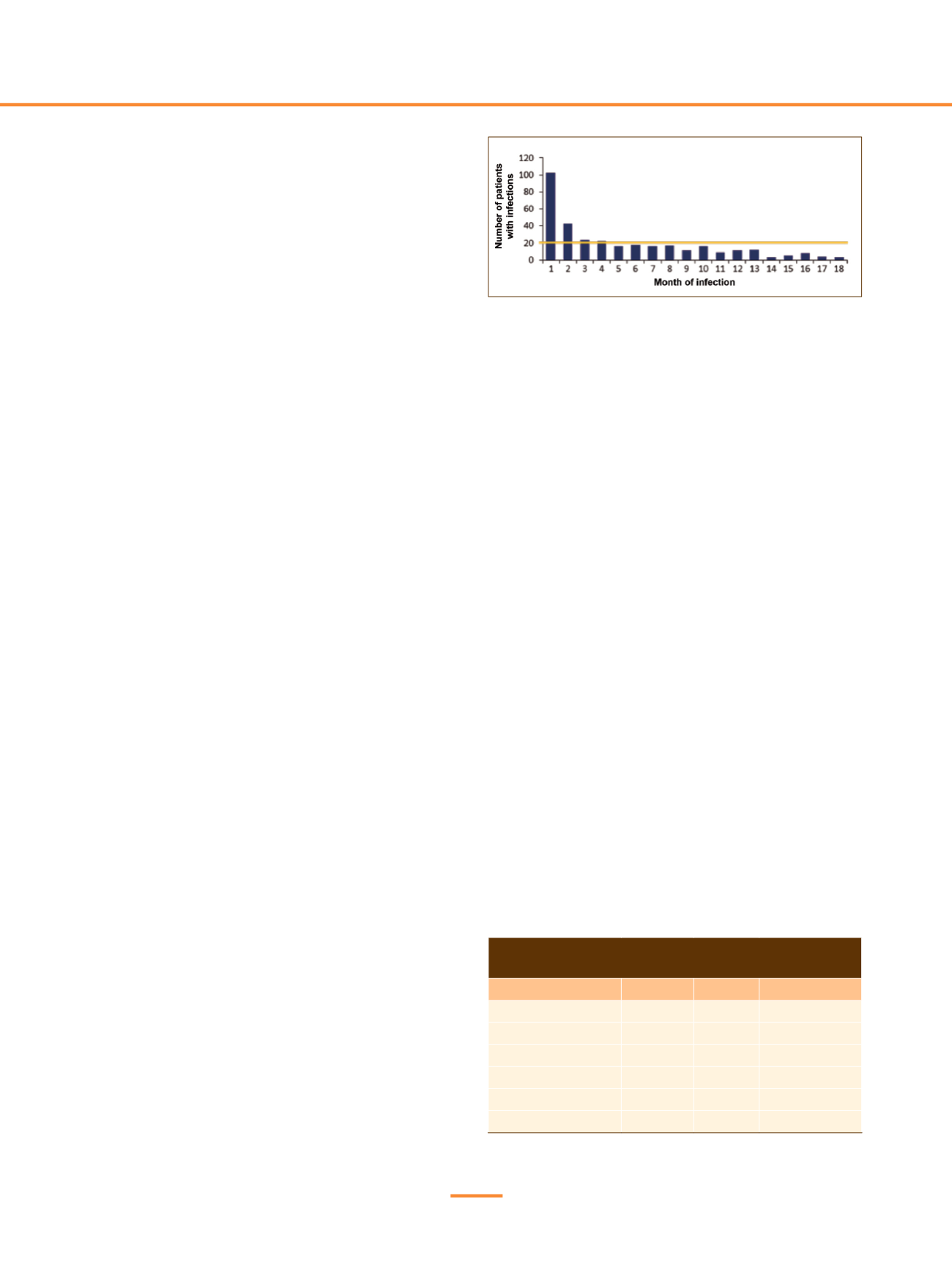
Resultados:
De los 1.623 incluidos en el estudio, 340 tenían
TE = grado 3 y 56,2% de estos (n = 340) presentaron su primera
infección en los primeros 4 meses
(Figura 1)
. El riesgo de in-
fección fue similar independientemente del brazo de tratamiento
(p = 0,53). Los factores de riesgo fueron evaluados en 1.378 pts,
y el modelo final identificó 4 variables (estado funcional según
Cooperative Oncology Group Este, ß2-microglobulina en suero,
lactato deshidrogenasa y hemoglobina), que se asociaron de for-
ma independiente con el grado TE = 3 infecciones que se produ-
cen en los primeros 4 meses
(Tabla 1)
.
Los grupos de alto y bajo riesgo definidos por el sistema de
puntuación
(Tabla 1)
se asociaron con tasas significativamente
diferentes de TE de grado = 3 infecciones durante los primeros
4 meses (24% y 7%, respectivamente).
Resumen:
El sistema de puntuación de riesgo que se describe
en el presente trabajo identifica a los pacientes con mayor riesgo
de infección durante los 4 primeros meses de tratamiento y pue-
de ser utilizado para implementar estrategias adaptadas al riesgo
para el tratamiento o la prevención de infecciones.
Tabla 1.
Multivariate logistic regression model for TE grade ≥ 3
infection with in the first 4 months
Model
Pr (>
ǀ
z
ǀ
)
Points
Infection risk
S
β
2M ≤ 3 mh/l
0.02135
-2
Lower
ECOG = 0
0.06231
-1
Lower
Hemoglobin ≤ 11 g/dl
0.07660
1
Higher
ECOG ≥ 2
O,01583
1
Higher
LDH ≥ 200 U/l
0.00299
1
Higher
S
β
2M ≤ 6 mh/l
3.09E-06
3
Higher
Figura 1.
Number of new patients with TE grade ≥ infections by month in
the first 18 months.



















