
XXXII Congreso Nacional de la Sociedad Española de Trombosis y Hemostasia
134
tor XIII, rituximab y ciclofosfamida. Actualmente se encuentra
bajo control ambulatorio, reiniciado el tratamiento anticoagulante
oral, con gran mejoría de los síntomas neurológicos y desaparición
de la clínica hemorrágica.
Conclusiones:
Se debe pensar en un déficit de factor XIII ante
un sangrado grave no explicada por otras circunstancias clínicas
o analíticas. El éxito del tratamiento radica en la rapidez en el
diagnóstico e instauración del tratamiento.
PC-402
Déficit combinado de factor XIII y alfa2-
antiplasmina adquirido y asociado a
diátesis hemorrágica
Díaz-Polo E. (1), Martín-Fernández L. (2), Caballero A. C. (1),
Vilalta N. (1), Ramírez L. (3), Vidal F. (3), Souto J. C. (1)
(1) Unitat d’Hemostàsia i Trombosi. Hospital de la Santa Creu i Sant Pau. Institut
d’Investigació Biomèdica Sant Pau (IIB-Sant Pau). Barcelona. (2) Unitat de
Genòmica de Malalties Complexes. IIB-Sant Pau. Barcelona. (3) Coagulopaties
congènites. Banc de Sang i Teixits. Barcelona. Unitat de Diagnòstic i Teràpia
Molecular. Vall d’Hebron Institut de Recerca. Universitat Autònoma de Barcelona
(VHIR-UAB). Barcelona
Introducción:
La deficiencia congénita de factor XIII (FXIII),
enzima de la cascada de la coagulación, y la deficiencia congéni-
ta del inhibidor de la fibrinólisis alfa2-antiplasmina (a2-AP), son
trastornos raros de transmisión autosómica recesiva asociados a
diátesis hemorrágica. Por otra parte, la deficiencia adquirida de
FXIII está asociada a enfermedades crónicas (renal, hepática),
síndromes linfoproliferativos y a algunos fármacos que en gene-
ral no condicionan sangrado significativo, mientras que el déficit
adquirido de a2-AP puede detectarse en pacientes con enfermedad
hepática severa, renal, coagulación intravascular diseminada, así
como receptores de terapia trombolítica.
Caso clínico:
Presentamos el caso clínico de un paciente de
90 años con historia de diátesis hemorrágica asociada a interven-
ciones quirúrgicas y traumatismos, aparecida desde los 88 años, sin
historia personal previa ni familiar de sangrado y con antecedentes
de hipertensión, hipercolesterolemia y enfermedad renal crónica
estadio III.
Métodos:
El diagnóstico clínico se realizó mediante hemo-
grama, estudio bioquímico y estudio hemostático. Además, para
el diagnóstico genético se realizó
Next Generation Sequencing
(NGS) mediante
TruSight One Sequencing Kit
(Illumina) en la
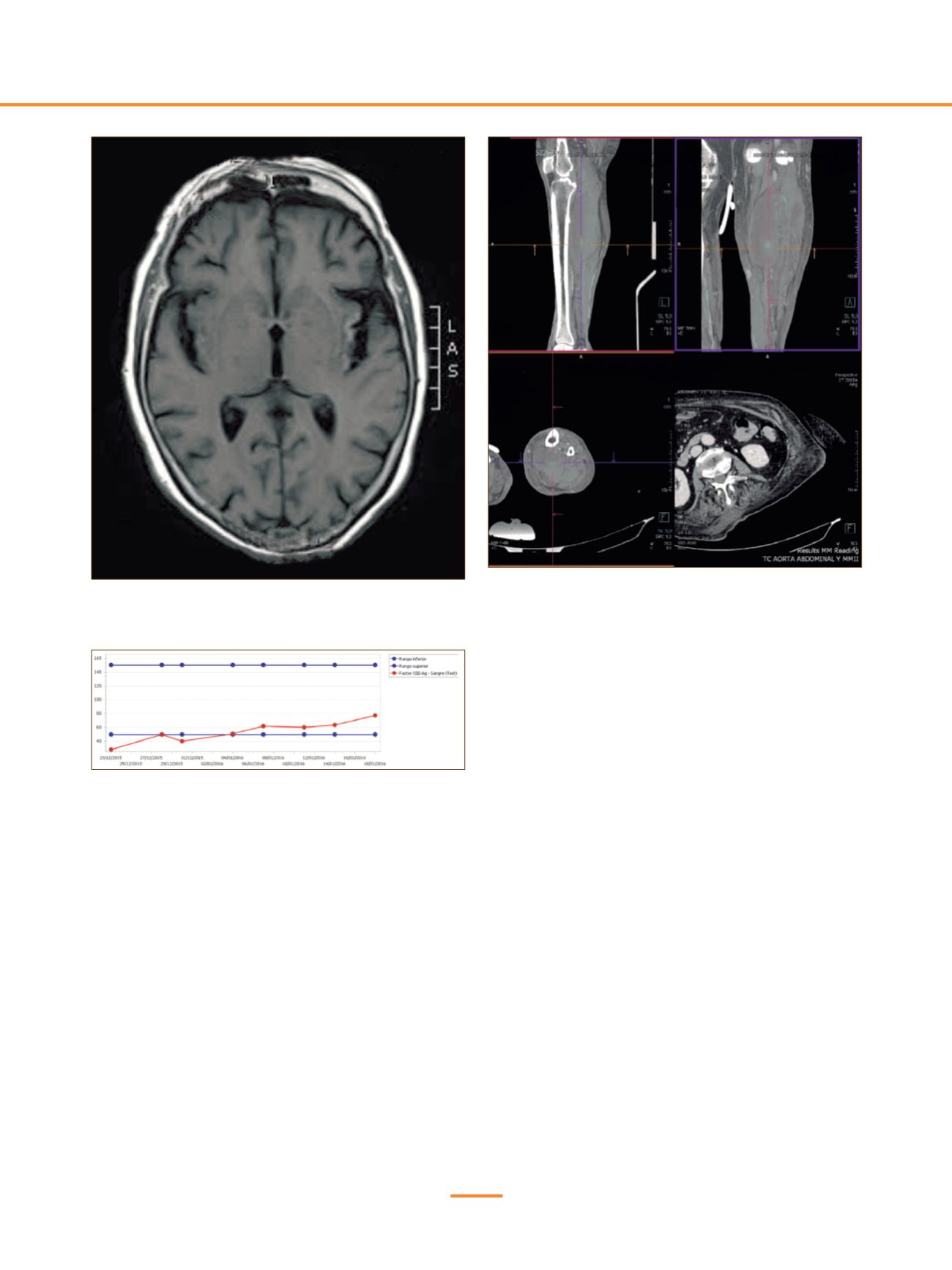
Figura 1.
Figura 2.
Figura 3.



















